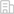1月10日,中國科學技術大學生命科學與醫學部翁建平教授團隊在Nature Cardiovascular Research期刊發表了題為“Endothelial IGFBP6 Suppresses Vascular Inflammation and Atherosclerosis”的研究論文。研究人員通過從體內到體外、從模式動物到患者等多維度開展了實驗研究,揭示了IGFBP6是減輕內皮細胞炎癥和預防動脈粥樣硬化性心血管疾病的潛在新靶點。血流剪切應力領域知名專家美國耶魯大學Martin A. Schwartz教授撰文“IGFBP6 contributes to vascular resilience”對此重點評論。
動脈粥樣硬化引起的心血管疾病(ASCVD)是全世界人類死亡的主要原因之一。炎癥是引起和加速ASCVD發生發展的重要機制。幾項具有里程碑意義的臨床試驗,比如CANTOS(N Engl J Med,2017)、COLCOT(N Engl J Med,2019)、LoDoCo2(N Engl J Med,2021)、RESCUE(Lancet,2021),以及2023年美國FDA批準低劑量秋水仙堿作為減少ASCVD患者心血管事件的第一種抗炎藥物,這些證據均表明靶向殘余炎癥風險對于ASCVD的治療至關重要。與此觀點一致的是:Ridker及其同事對31,245名接受他汀類藥物治療的患者進行了分析,發現hs-CRP評估的殘余炎癥風險比LDL-C評估的殘余膽固醇風險更能預測未來心血管事件和死亡的風險(Lancet,2023)。因此,尋找抵抗血管炎癥的新靶點有望為治療ASCVD帶來新希望。
研究人員從GEO公共數據庫中選擇了具有動脈粥樣硬化保護效果的干預(他汀類藥物或層流剪切應力)測序數據集,以及動脈粥樣硬化患者斑塊的基因表達數據集,發現胰島素樣生長因子結合蛋白6(IGFBP6)可能是一種潛在的血管穩態相關分子。已有研究表明,IGFBP6在調節細胞周期、增殖、細胞遷移等方面發揮著至關重要的作用。然而,IGFBP6在內皮穩態和動脈粥樣硬化中的確切作用和機制尚不清楚。
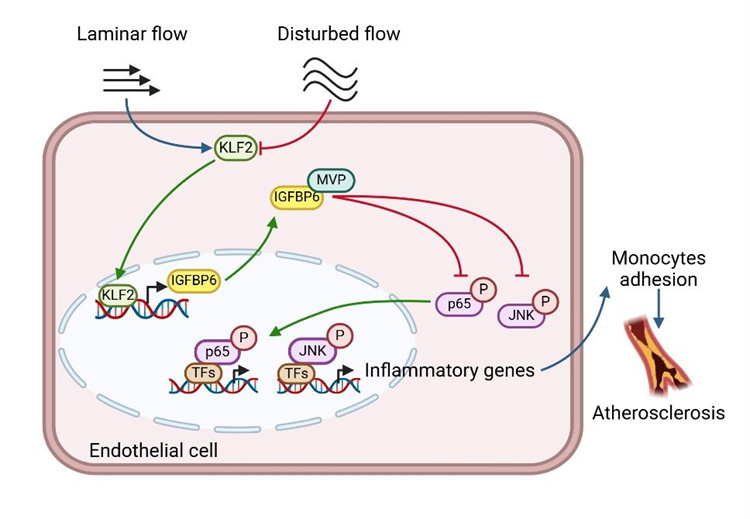
IGFBP6保護內皮功能與動脈粥樣硬化的機制示意圖
研究人員證明IGFBP6水平在人類動脈粥樣硬化斑塊和冠心病患者血清中顯著降低。內皮細胞中敲低IGFBP6會增加炎癥分子的表達和單核細胞的粘附。同時,由湍流和TNF介導的促炎作用被IGFBP6的過表達所逆轉。機制研究進一步揭示,IGFBP6在轉錄上受krüppel樣因子2(KLF2)調節,并通過主拱頂蛋白(MVP)-c-Jun N-末端激酶(JNK)/核因子κB(NF-κB)信號軸發揮抗炎作用。動物表型方面,IGFBP6的全身或內皮特異性缺失加速了飲食誘導的小鼠動脈粥樣硬化,而IGFBP6的內皮特異性過表達改善了小鼠的動脈粥樣硬化。基于這些發現,研究人員認為內皮IGFBP6的減少是血管炎癥和動脈粥樣硬化的誘發因素,內皮IGFBP6可作為治療靶點。
綜上所述,本研究表明IGFBP6響應血流剪切應力并具有抗內皮炎癥和動脈粥樣硬化的作用,有希望成為治療動脈粥樣硬化和泛血管疾病的新靶點。
中國科學技術大學生命科學與醫學部博士研究生蘇美名、博士研究生趙玟淇和課題組博士后蔣輝為該論文的共同第一作者,翁建平教授與徐索文研究員為本論文的共同通訊作者。復旦大學附屬中山醫院葛均波院士,美國羅切斯特大學Bradford C. Berk教授,埃默里大學Hanjoong Jo教授,英國倫敦瑪麗女王大學Paul C Evans教授,弗吉尼亞州大學Clint L. Miller教授, 芝加哥大學Yun Fang教授,德國馬普心肺研究所Stefan Offermanns院士,波蘭羅茲醫科大學Maciej Banach教授,蘇州大學唐朝君教授、朱力教授,香港城市大學黃聿教授、王力教授,中國科學技術大學生命科學與醫學部曾筑天教授等均給予了重要幫助。該工作得到了科技部重點研發計劃,國家自然科學基金,中國科大附一院創新攻關團隊項目等資助,以及代謝健康與泛血管病安徽省重點實驗室、中國科學技術大學內分泌與代謝病研究所的大力支持。